重水の氷は水(軽水)に浮く? 沈む?
2021/05/01
結論:重水の氷は軽水の水では沈む
氷の比重は水の状態の比重より軽くなるので水に浮きます。
重水の氷も重水の水より軽くなるので、重水の水には浮きます。
重水は比重が軽水より重いけれども、凍って比重が軽くなったら、
軽水の水に浮くのか?、沈むのか?。
実験結果と理論解説します。
下図のように重水の氷は軽水の水では沈みます。
重水の氷も重水の水より軽くなるので、重水の水には浮きます。
重水は比重が軽水より重いけれども、凍って比重が軽くなったら、
軽水の水に浮くのか?、沈むのか?。
実験結果と理論解説します。
下図のように重水の氷は軽水の水では沈みます。

その理屈は
1.分子構成の違い
2.質量(重さ)が違う理由
3.氷になったときの比重(体積増加の割合)
4.軽水と重水の違い
1.水の分子構成と質量(重さ)
軽水:通常の水
化学式 :H2O
モル質量: 18.01528 g/mol
密度: 0.997 g/cm³
重水:通常の水の水素が重水素に置き換わった水で、通常の水より重い
化学式 :D2O
モル質量: 20.0276 g/mol
密度: 1.11 g/cm³
化学式 :H2O
モル質量: 18.01528 g/mol
密度: 0.997 g/cm³
重水:通常の水の水素が重水素に置き換わった水で、通常の水より重い
化学式 :D2O
モル質量: 20.0276 g/mol
密度: 1.11 g/cm³
軽水と重水の模式図
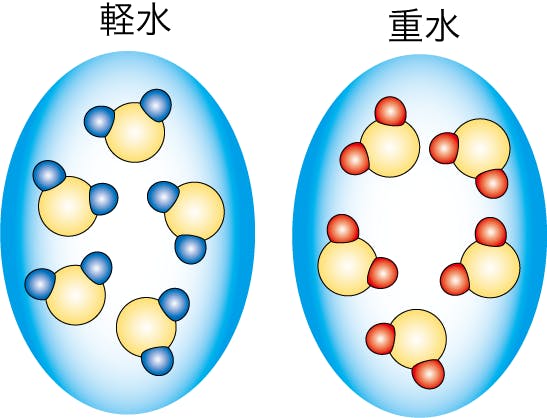
質量(重さ)が違う理由
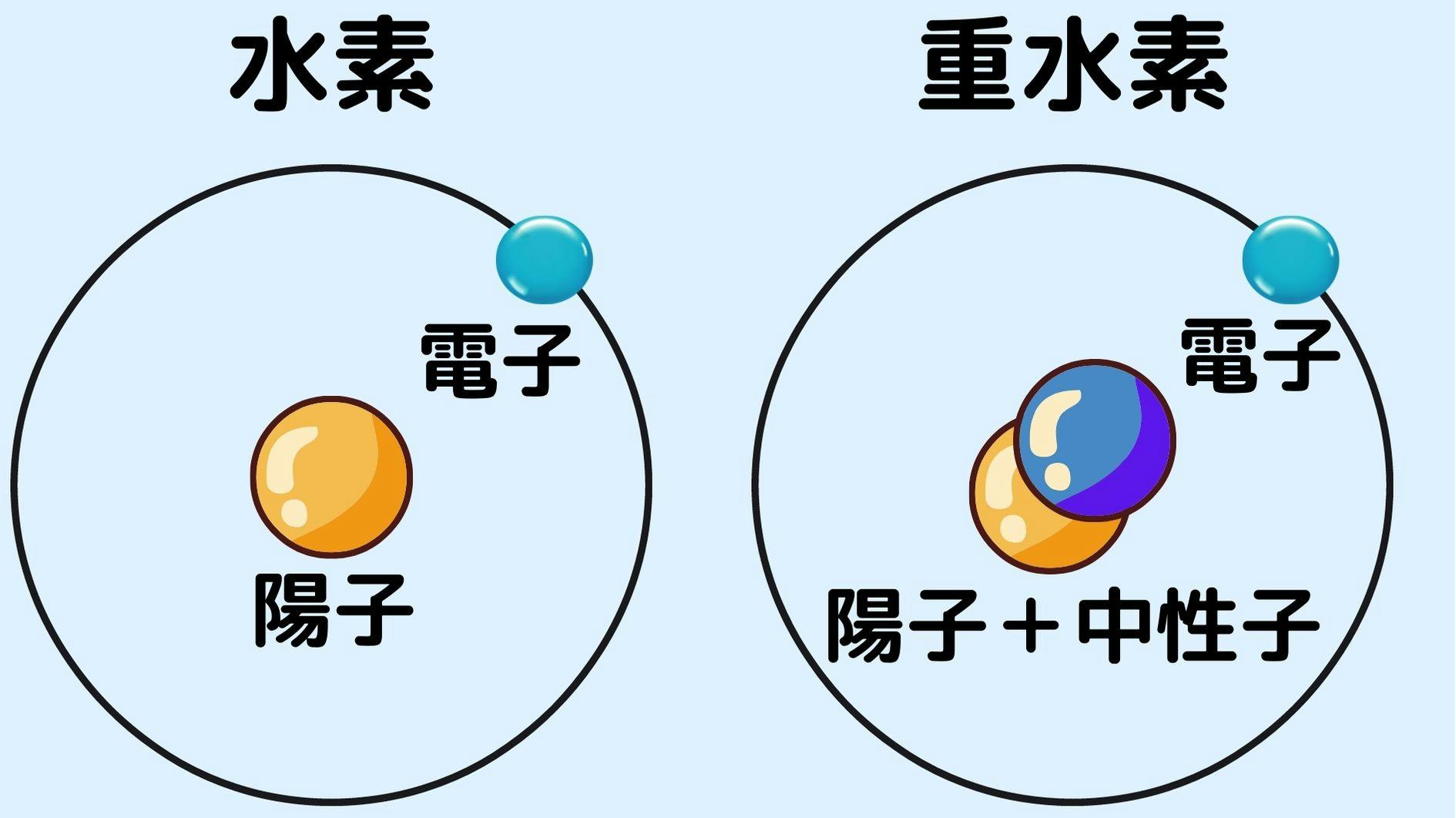
水素の原子核の構成の違いが質量の違う理由
水素原子:H、1個の陽子を含む原子核と1個の電子で構成
重水素原子:D、1個の陽子と1個の中性子を含む原子核と1個の電子で構成
水素原子:H、1個の陽子を含む原子核と1個の電子で構成
重水素原子:D、1個の陽子と1個の中性子を含む原子核と1個の電子で構成
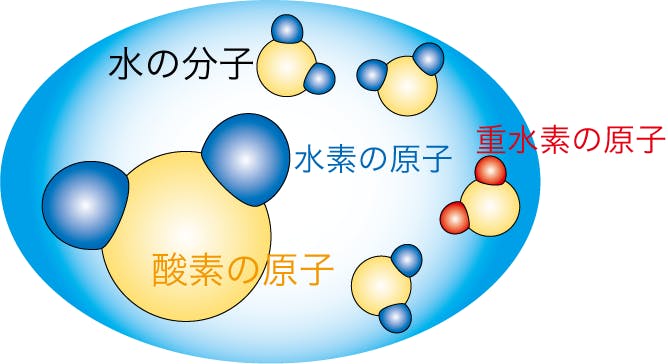
2.軽水と重水の質量(重さ)比較
(分子の構成比較)
分子の重さは原子核の構成でほぼ決まる。(電子の質量(重さ)は微量なので無視しても影響ない)
(中性子が陽子より少し重いが同じとして計算しても通常は問題無い。)
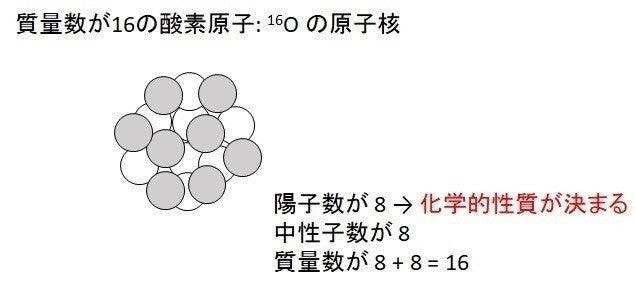
軽水:H2O 水素2個+酸素1個
質量=水素(陽子1個)*2 + 酸素(陽子8個+中性子8個)
=陽子10個+中性子8個
=陽子18個分
重水:D2O 重水素2個+酸素1個
質量=重水素(陽子1個+中性子1)*2 + 酸素(陽子8個+中性子8個)
=陽子10個+中性子10個
=陽子20個分
質量比(重量比)
重水/軽水=20/18=1.1111
(中性子が陽子より少し重いが同じとして計算しても通常は問題無い。)
軽水:H2O 水素2個+酸素1個
質量=水素(陽子1個)*2 + 酸素(陽子8個+中性子8個)
=陽子10個+中性子8個
=陽子18個分
重水:D2O 重水素2個+酸素1個
質量=重水素(陽子1個+中性子1)*2 + 酸素(陽子8個+中性子8個)
=陽子10個+中性子10個
=陽子20個分
質量比(重量比)
重水/軽水=20/18=1.1111
3.氷になったときの比重(体積増加の割合)
水に対する氷の比重が0.917、体積が約10%増加します。
水が0.00℃以下(1気圧下)になると、運動するための熱エネルギーが極端に低く、水分子は動きをとめて互いに結合します。(氷になる)
氷になると
水分子は、曲がった形をしているために、分子同士はすきまが多い形でしか結合できません。
そのために、分子と分子の間にすきまができて距離があき、その分体積が増えることになります。水を凍らせるとかさが増えるのは、そのためなのです(増える量は、約10パーセント)
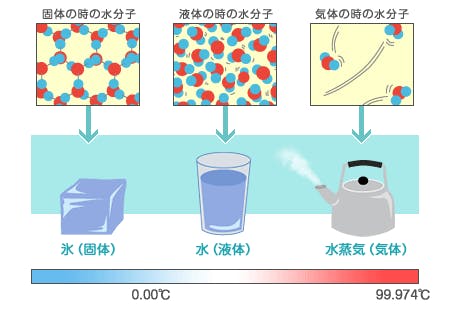
水の分子は、化学記号からわかるとおり水素原子(H)2つと酸素原子(O)1つが結合してできていますが、この水分子1つでは液体になりません。
水という液体になるためには、水分子がたくさん連なることが必要です。
水分子の場合は酸素側がマイナスの電荷、水素側がプラスの電荷を持つようになり、いわば磁石のような働きを持っているために、正負で引き合う電気的な力によって結合します(水素結合)。
この水素結合により、水分子がつながり、水分子の集合(水クラスター)が形成されます。
常温の水では、5~6個から十数個の分子がクラスタを形成しています。
水が0.00℃以下(1気圧下)になると、運動するための熱エネルギーが極端に低く、水分子は動きをとめて互いに結合します。(氷になる)
氷になると
水分子は、曲がった形をしているために、分子同士はすきまが多い形でしか結合できません。
そのために、分子と分子の間にすきまができて距離があき、その分体積が増えることになります。水を凍らせるとかさが増えるのは、そのためなのです(増える量は、約10パーセント)
水の分子は、化学記号からわかるとおり水素原子(H)2つと酸素原子(O)1つが結合してできていますが、この水分子1つでは液体になりません。
水という液体になるためには、水分子がたくさん連なることが必要です。
水分子の場合は酸素側がマイナスの電荷、水素側がプラスの電荷を持つようになり、いわば磁石のような働きを持っているために、正負で引き合う電気的な力によって結合します(水素結合)。
この水素結合により、水分子がつながり、水分子の集合(水クラスター)が形成されます。
常温の水では、5~6個から十数個の分子がクラスタを形成しています。
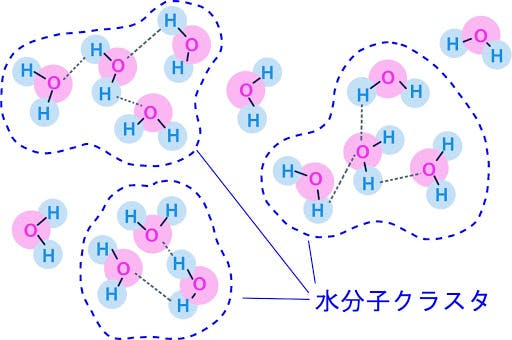
水(液体(左))と 氷(固体(右))の模式図

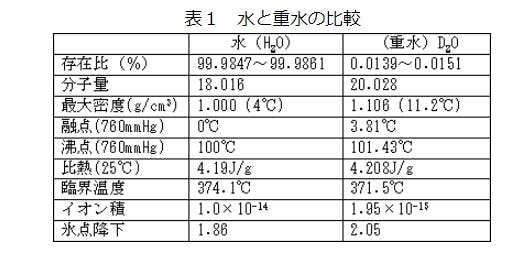
4.軽水と重水の違いは
軽水(実際上、通常の水と考えてよい)と重水D2Oは同じように無色透明で、屈折率もあまり変わりがありませんので、見かけはほとんど差がありません。
また化学的な反応性や溶媒としての性質にも差がありません。
物理的特性(質量、融点、沸点、密度(比重)等)と
生体への影響 は少し違います。
また化学的な反応性や溶媒としての性質にも差がありません。
物理的特性(質量、融点、沸点、密度(比重)等)と
生体への影響 は少し違います。
生体への影響
【重水は動植物に悪影響を与えます。】
重水は生物の細胞活動を阻害する物質です。
普通の水のように飲んでしまい、水分摂取量の10%を超えると影響があらわれ、50%に達すると死亡すると考えられています。
(他の生物で得られたデータからの推測)
飲料水などとして大量に摂取すると酵素反応などの生体内反応に失調をきたす。
哺乳類の場合25パーセント重水は不妊を引き起こし、50パーセント重水は致死的である。
人間の場合、
水分摂取量の10パーセントを超えると問題が生じるとの推測がある。
重水の中では魚類も生きることができず、植物の発芽や成長も停止する。
一方、藻類やバクテリアは100パーセント重水の中でも生息可能である。
「健康寿命を延ばす」
その願いをかなえます
その願いをかなえます
国が認め、メディアでも大きな話題になりました。
テロメア解説動画
クラブエターナルライフ公式動画_Lifelength社

